重要なポイント
社内解析では、NovaSeq XシリーズをUltima Genomics UG 100プラットフォームと比較して評価しました。この評価により、NovaSeq Xシリーズは以下であることがわかりました:
- NovaSeq Xシリーズは完全なNIST v4.2.1ベンチマークに対してWGSの正確性を測定し、Ultima Genomicsはゲノムの4.2%を除外するサブセットに対してUG 100プラットフォームを使用してWGSの正確性を測定します。
- 完全なNIST v4.2.1ベンチマークに対して評価した場合、UG 100プラットフォームと比較してSNVエラーが1/6に、Indelエラーが1/22に減少します。
- UG 100プラットフォームがUltima Genomics高信頼領域のみを分析する場合と比較して、約180,000以上のSNVと270,000以上のインデルでゲノム全体を解析します。
- UG 100プラットフォームと比較して、GCリッチなシーケンスや10塩基対を超えるホモポリマーを含む反復ゲノム領域で高いカバレッジとバリアントコール正確性を維持します。
- UG 100プラットフォームと比較して、生物学的に関連する遺伝子に関するより多くの洞察を提供
Ultima Genomicsとイルミナのシーケンスプラットフォームの比較
イルミナは、次世代シーケンサー(NGS)機能の革新と将来の手法の構築に絶え間ない取り組みを続けてきました。1 NovaSeq Xシリーズは、データ集約型アプリケーションを生産規模で実現し、科学者が新たな発見を行えるよう支援します。過去10年間、Ultima Genomicsのような新興企業はNGSプラットフォームを導入してきました。2024年、Ultima GenomicsはUG 100シーケンスプラットフォームを大胆な主張で立ち上げました。これには、バリアントコールにおいて業界をリードする正確性で年間20,000のヒトゲノムをシーケンスできるという主張が含まれます。2これらの性能と正確性の主張を評価するために、イルミナはNovaSeq XシリーズとUG 100プラットフォームの比較解析を実施しました。この解析結果から、NovaSeq Xシリーズは、UG 100プラットフォームよりも、より正確なバリアントコーリングを実現し、より高品質でより包括的なゲノムを提供し、疾患の分子メカニズムに対するより多くの洞察を可能にすることが実証されました。
Ultima Genomicsとイルミナを比較するデータソース
NovaSeq X Series 10B Reagent Kitを使用してNovaSeq X Plus Systemでイルミナ全ゲノムシーケンス(WGS)データを生成し、続いてDRAGEN v4.3二次解析を行いました。データはカバレッジ深度が1/35にダウンサンプリングされました(重複を含む)。Ultima Genomics WGSデータは、UG 100プラットフォームで重複を除いた40倍のカバレッジ深度で生成されたバリアントコールフォーマット(VCF)で公開データセット からリリースされ、Ultima GenomicsのDeepVariantソフトウェアを使用して解析しました。
NovaSeq Xシリーズでバリアントコールの正確性を向上
米国国立標準技術研究所(NIST)v4.2.1のGenome in a Bottle(GIAB)HG002リファレンスゲノムのベンチマークは、WGSおよびバリアントコーリング解析ツールの正確性と性能を評価するために使用されています。3,4 NIST v4.2.1ベンチマークには、1塩基変異(SNV)の信頼性の高いジェノタイプコール、挿入と欠失(indel)、および構造多型(SV)、セグメント重複で構成される困難な領域とともに、低結合性領域、生物学的に関心のある遺伝子を含むことができる反復配列が含まれます。4,5
イルミナはDRAGEN二次解析によりNovaSeq Xシリーズで得られたWGSの正確性を、すべてのゲノム領域を含む完全なNIST v4.2.1ベンチマークに対して測定します(図1)。6逆に、Ultima Genomicsは、NIST v4.2.1ベンチマークの定義されたサブセットに対してUG 100プラットフォームでWGSの正確性を測定します。このサブセットはUG「High-Confidence Region」(HCR)と呼ばれます。UG HCRは、ホモポリマー、反復シーケンス、カバレッジの低い領域(図1)など、UG 100プラットフォームで性能の低い領域をマスクします。7重要な点として、UG HCRから除外される領域には、NISTベンチマークバリアントの4.2%が含まれます。

図1:Ultima Genomics HCRはゲノムの4.2%をマスク-NovaSeq XシリーズのWGS正確性は完全なNIST v4.2.1ベンチマークに対して測定されますが、UG HCRはゲノムの4.2%を解析から除外します。
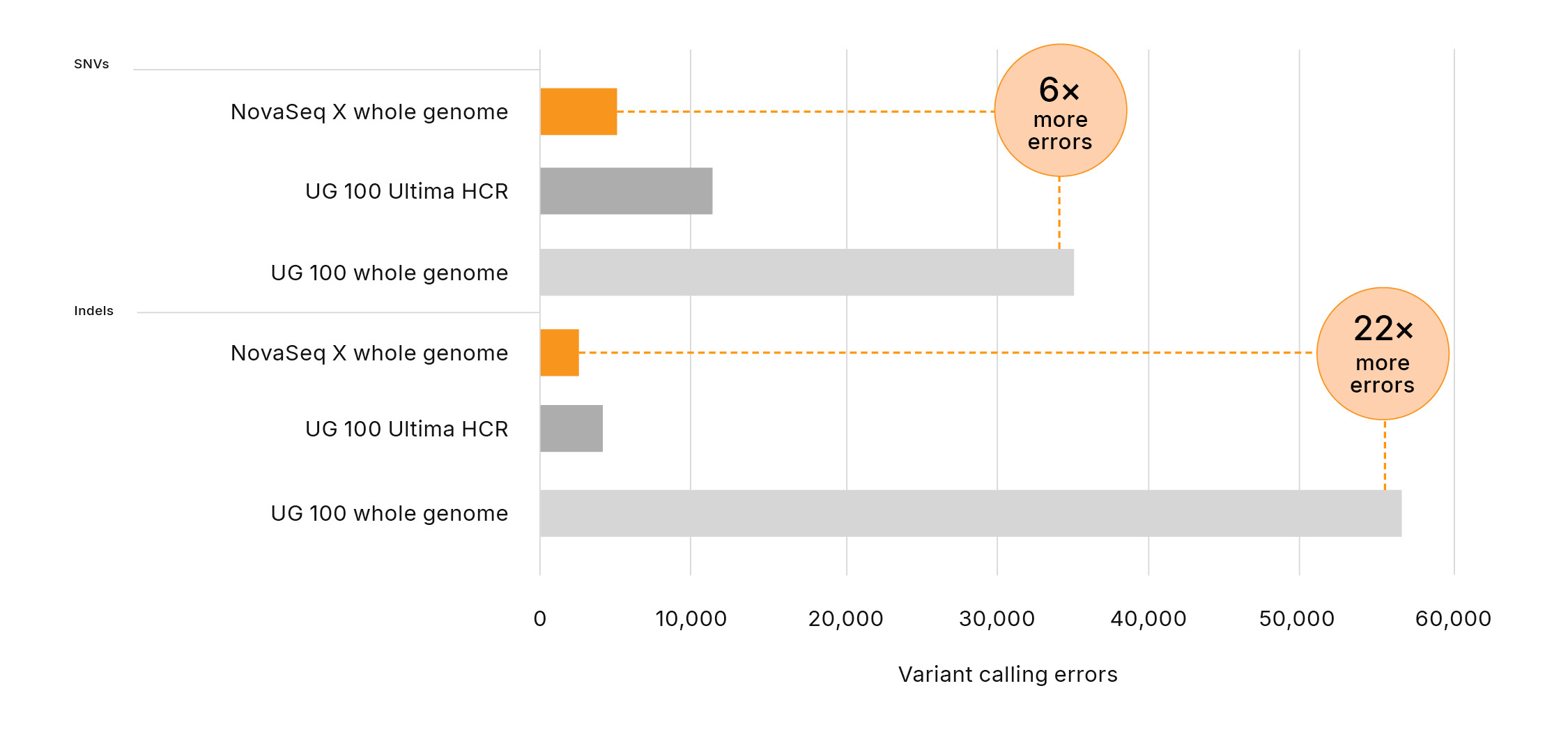
図2:Ultima Genomicsによるバリアントコールのエラーが有意に多い─UG 100プラットフォームでは、NIST v4.2.1の全ベンチマーク領域に対して評価されたNovaSeq Xシリーズと比較して、SNVおよびインデルのバリアントコールのエラーがそれぞれ6倍および22倍多くなっています。エラーは、偽陽性と偽陰性の合計数として定義されます。

図3:Ultima Genomics HCRは、主要なバリアントをマスク─UG 100プラットフォーム上のWGSのUG HCRへの解析を制限することで、NovaSeq Xシリーズと比較してSNVとインデルのバリアントコールが少なくなります。
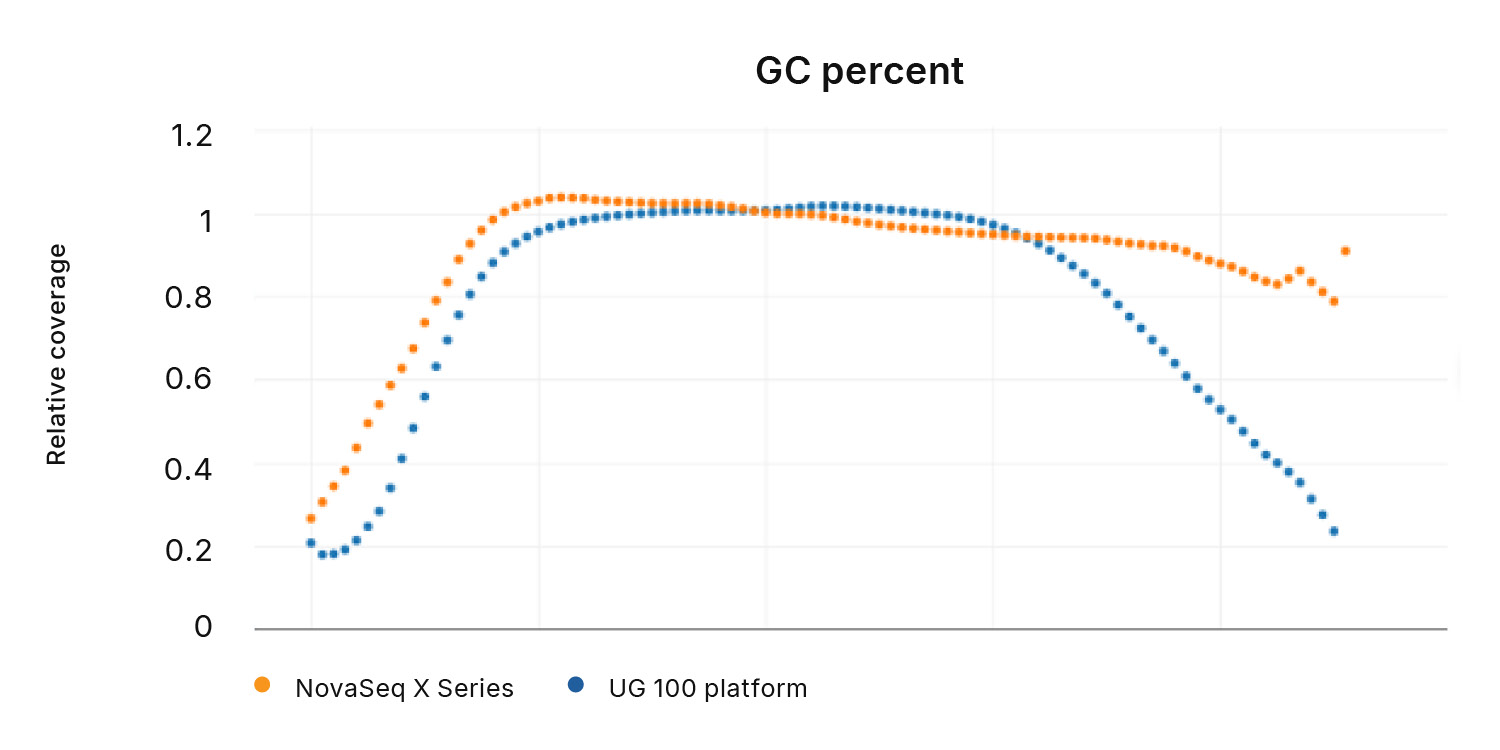
図4:Ultima Genomicsを使用したGCリッチ領域のカバレッジの喪失─UG 100プラットフォームはNovaSeq Xシリーズと比較して、ゲノムの反復的でGCリッチな領域のカバレッジを喪失します。
NovaSeq Xシリーズによるゲノムカバレッジの向上
NovaSeq Xシリーズのイルミナシーケンシングは、SNVの99.94%*、コピー数バリアント(CNV)の97%†、SVの88%ǂ、ショートタンデムリピート(STR)の95.2%§、98%の一致率で医学的に関連する遺伝子を少なくとも13のターゲット遺伝子コーラー、¶94%の一致率でヒト白血球抗原(HLA)タイピングを正確にコールする包括的で高品質のゲノムを提供します。**
* rtg vcfevalを用いたHG002 NIST v4.2.1との比較。
† wittyer v0.4.1を用いたHG002 NIST v0.6(hg38)との比較。
ǂ Truvari v.4.2.2を用いたHG002 NIST T2T Q100 v1.1_v0.019(hg38)との比較。
§ 28 STR遺伝子座は、359のサンプル(少なくとも1つの遺伝子座における拡大した157のサンプル)の評価に含まれました。
¶ 公開された技術論文から調達された直交技術に対する一致メトリクス。
** The 1000 Genomes Projectの3202の多様なWGSサンプルに対するT1Kとの比較。
対照的に、Ultima Genomicsは、UG HCRに依存したUG 100のWGSの正確性を評価することで、性能の欠陥をマスクします。Ultima Genomicsシーケンス技術を使用して信頼性の低い性能と信頼性を示すNIST v4.2.1ベンチマークの領域は除外されます。UG HCRに解析を制限するとコールされない多数のバリアント(約450,000)は、(図3)どのデータが見逃される可能性があるかの不確実性を強調しています。
UG HCRによって除外された領域はゲノムの4.2%に相当し、エクソームの2.3%、ClinVarバリアントの1.0%が含まれます。これらの除外領域もゲノムCNVの5.1%、ClinVar CNVの4.7%を占めています。合わせると、793遺伝子の病原性バリアントはUG HCRから除外されるため、関連する疾患に対する洞察が制限されます。さらに、Ultima Genomicsは、ホモポリマーによるシーケンス中にSNVとインデルのバリアントコーリング正確性が高いと主張していますが、内部解析では、UG 100プラットフォームのインデル正確性はNovaSeq Xシリーズと比較して、10塩基対より長いホモポリマーでは有意に低下したことが示されました(図5)。実際、UG HCRは12塩基対を超えるホモポリマー領域を除外しています。7 公表された研究では、ホモポリマーリピート長がヌクレオソームの位置を変えることで近くの遺伝子の発現を調節する可能性があることが示されており、8 Ultima Genomics解析からこれらの領域を除外すると、生物学的に関連性のある貴重な洞察が見逃される可能性があります。
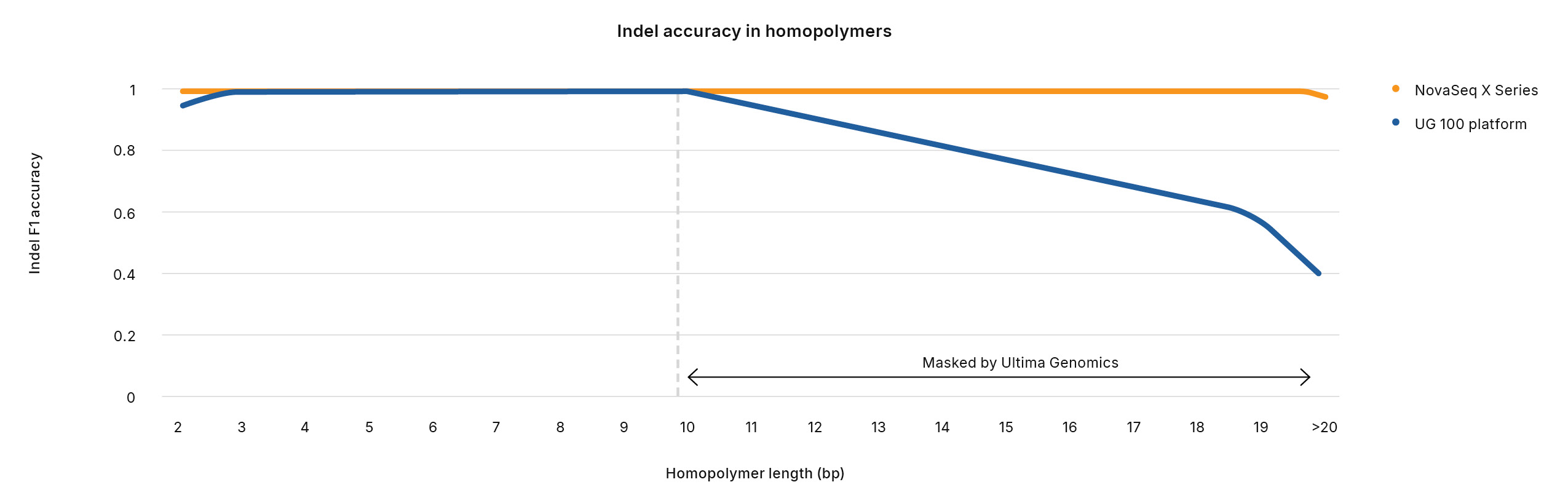
図5:NovaSeq Xシリーズと比較して、Ultima Genomicsによるインデル正確性の低下─UG 100プラットフォームによるインデル正確性は、10塩基対を超えるホモポリマーでは大幅に低下します。
NovaSeq Xシリーズで生物学的により妥当性のある洞察を得る
UG HCRから除外されるゲノム領域には、疾患関連遺伝子における機能的に重要な遺伝子座、免疫形質や神経形質に関連するSTRリッチ遺伝子が含まれます(表1)。一例として、B3GALT6遺伝子があります。これは、グリコサミノグリカン(GAG)の合成に重要な酵素をコードしています。B3GALT6のバリアントは、Ehlers-Danlos症候群と関連付けられています。9別の例は、脆弱なXメッセンジャーリボ核タンパク質1(FMR1)遺伝子です。これは正常な脳の発達と生殖機能に不可欠です。FMR1の変異は、脆弱なX症候群を引き起こします。10 B3GALT6とFMR1の両方にGCリッチなシーケンスがあり、UG 100プラットフォームでのカバレッジが失われたため、これらの遺伝子の病原性バリアントおよび可能性のある病原性バリアントが除外される可能性があります(図6A, 6B)。さらに、BRCA1腫瘍抑制遺伝子のバリアントは、個人が乳がんを発症しやすい素因となる十分に確立された関連性があります。11,12しかし、病原性BRCA1バリアントの1.2%はUG HCRから除外されており、UG 100プラットフォームでのシーケンスでは、NovaSeq Xシリーズと比較してBRCA1遺伝子のIndelコールエラーが有意に多く発生しました(図6C)。
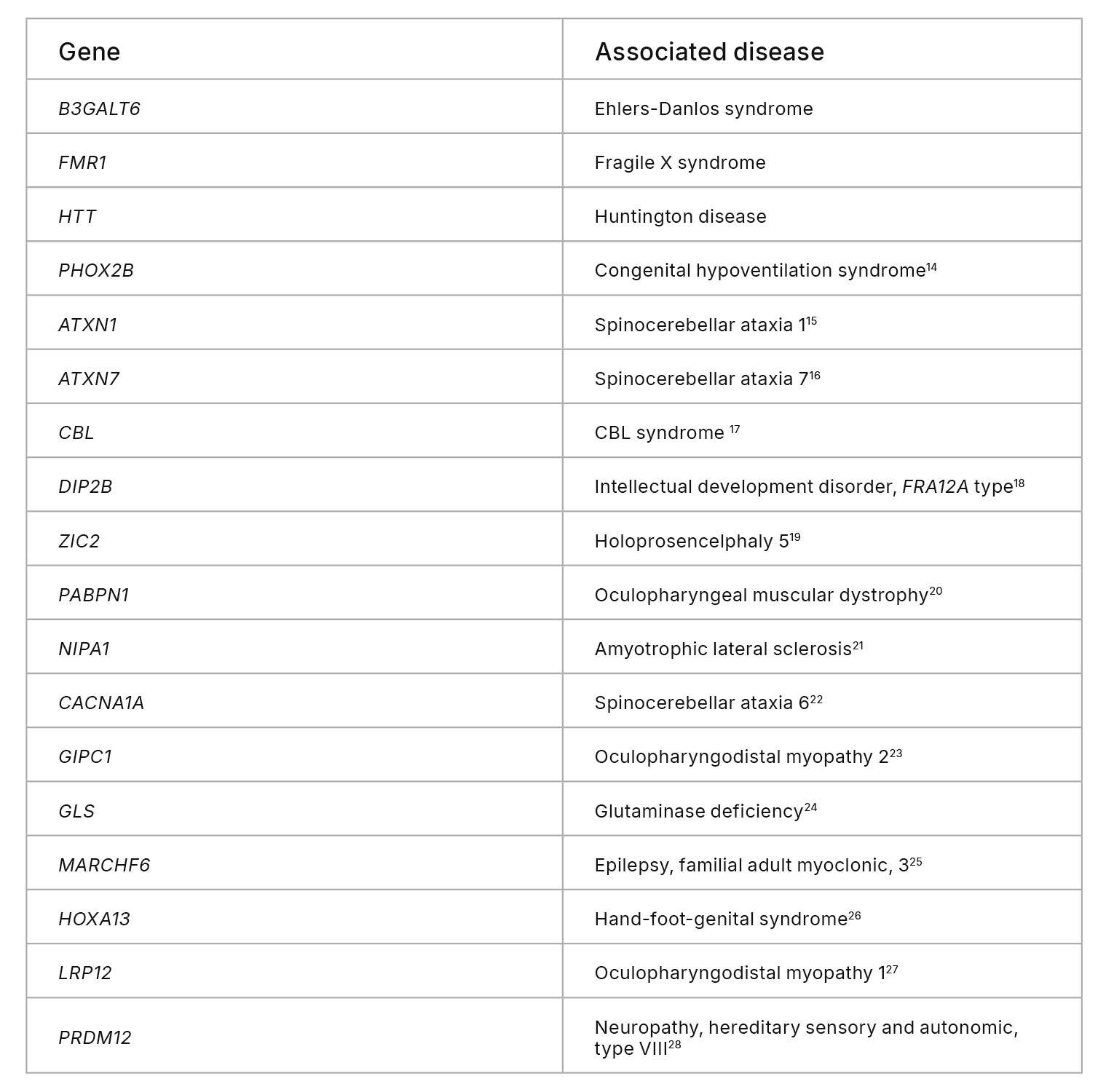
表1:UG HCRから除外された生物学的に関連する遺伝子

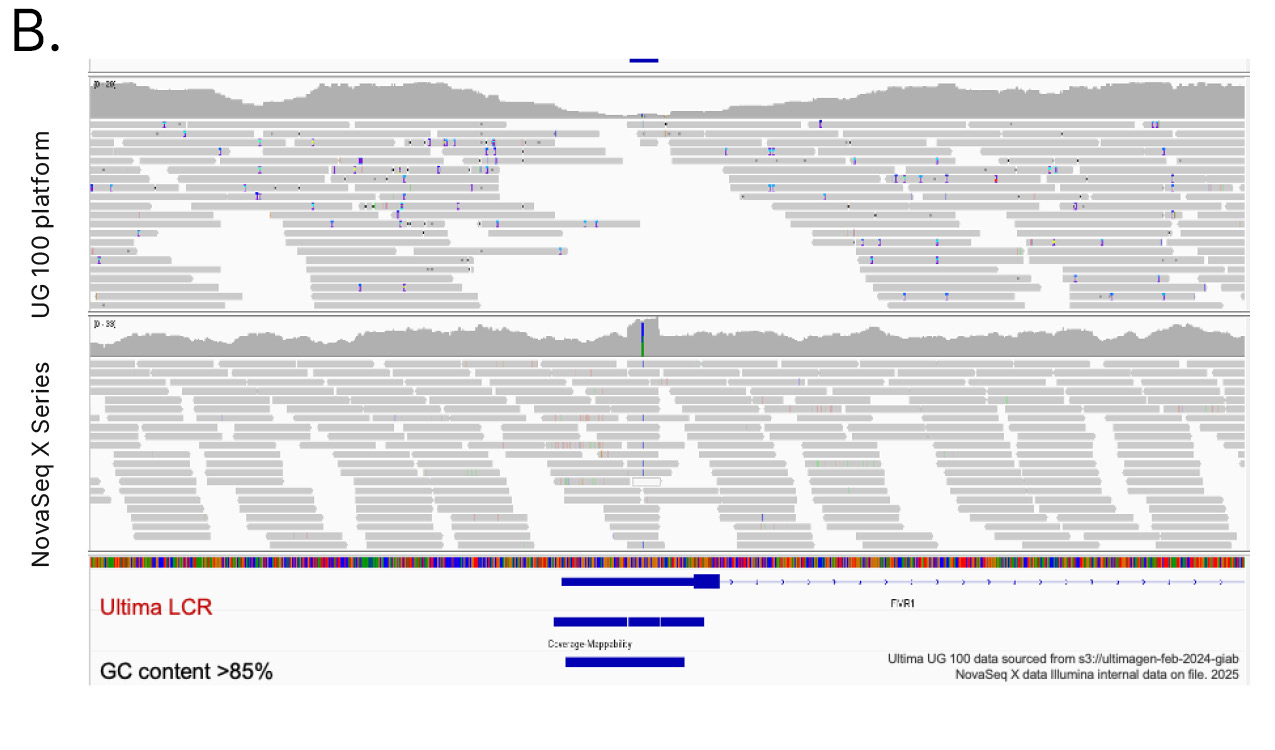
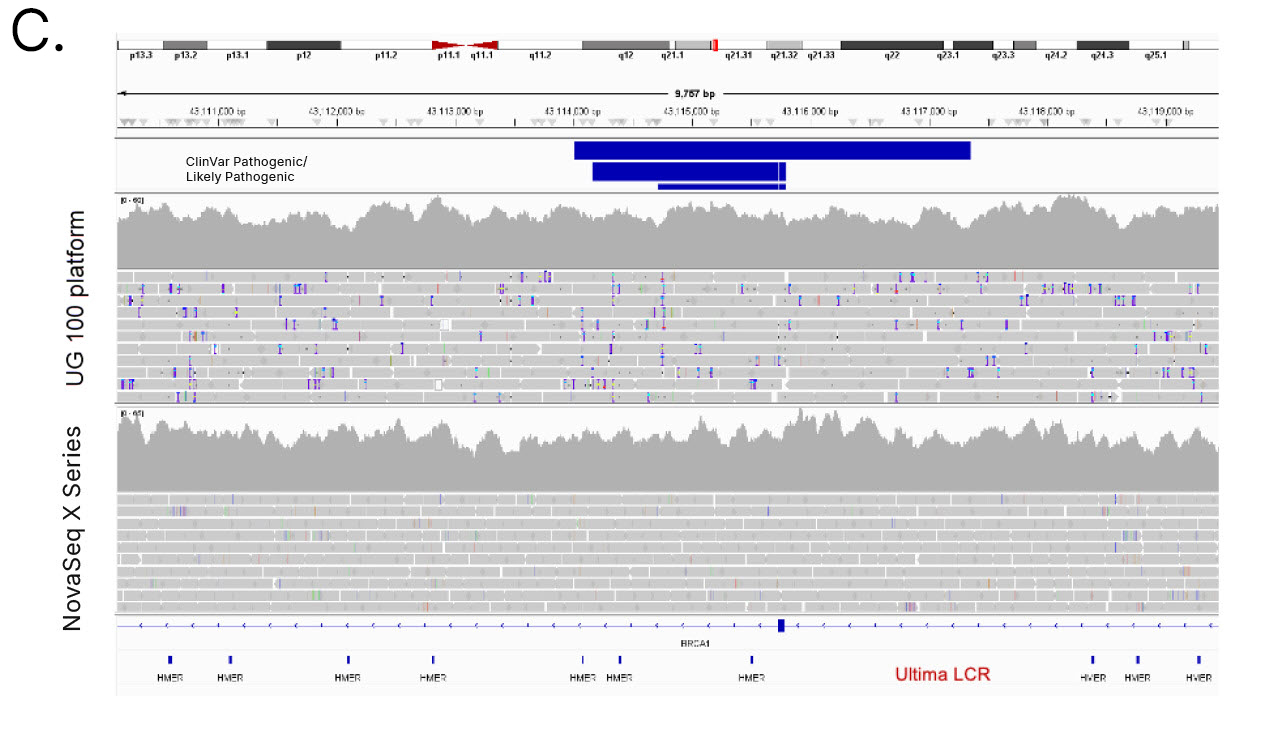
図6:Ultima Genomicsによるカバレッジの喪失─UG 100プラットフォームによるシーケンスでは、(A)B3GALT6および(B)FMR1、および(C)NovaSeq Xシリーズと比較してBRCA1遺伝子のIndelコールエラーが有意に多いなどのGC含有量が高い疾患関連遺伝子のカバレッジの喪失が生じます。
まとめ
Ultima GenomicsとIllumina NGSプラットフォームを評価した結果、WGS用のUG 100プラットフォームと比較してNovaSeq Xシリーズの優れた性能が実証されました。NovaSeq Xシリーズは、より高い正確性を実現し、困難な領域を含むゲノム全体の包括的なカバレッジを提供します。UG 100プラットフォームの性能は、Ultima Genomicsの「信頼性の高い領域」によって強化されています。この領域は、プラットフォームの性能が低い解析からゲノムの4.2%を除外します。NovaSeq Xシリーズは、生物学的に関連する遺伝子に生物学的洞察をもたらすために必要な正確性とゲノムカバレッジを生成しますが、UG 100プラットフォームでは、B3GALT6やBRCA1などの疾患との関連が知られている遺伝子を正確にシーケンスすることはできません。
本論文で確立されたように、Ultima Genomicsは、優れたカバレッジと正確性を主張するために、さまざまなゲノム領域を解析から除外しています。UG 100プラットフォームの新規バリアントの発見や、関連する遺伝子の既知のバリアントの検出能力は限られています。これとは対照的に、イルミナは27年にわたる専門知識を持つ信頼できるグローバルリーダーであり、包括的なサポートとクラス最高の製品の一貫性を提供し続け、NGSソリューションの基準を確立しています。NovaSeq XシリーズとDRAGEN二次解析は、Ultima Genomicsテクノロジーに必要な妥協点やトレードオフなしに、包括的なWGSに大規模な正確性と品質を提供します。
関連リンク
WGSについてご質問がありますか?
イルミナのプラットフォームとUltima Genomicsの比較についてご質問がありますか? 総所有コストの決定をお手伝いし、お客様のセットアップに最適なソリューションを提案します。
参考文献
- Illumina. 25 greatest impacts in 25 years: Illumina and the evolution of genomics. illumina.com/company/news-center/feature-articles/25-greatest-impacts-in-25-years--a-look-back-at-illumina-and-the.html. 2023年4月3日発表。アクセス日:2025年7月22日
- Business Wire. Ultima announces UG 100 and reveals disruptive cost and accuracy profile to enable the era of the $100 genome and beyond. businesswire.com/news/home/20240206310974/en/Ultima-Announces-UG-100-and-Reveals-Disruptive-Cost-and-Accuracy-Profile-to-Enable-the-Era-of-the-%24100-Genome-and-Beyond. 2024年2月6日発表。アクセス日:2025年7月22日
- Daniels CA, Abdulkadir A, Cleveland MH, et al. A robust benchmark for detecting low-frequency variants in the HG002 Genome In A Bottle NIST reference material. Preprint. bioRxiv. 2024;2024.12.02.625685. 2024年12月5日発表。 doi:10.1101/2024.12.02.625685
- Wagner J, Olson ND, Harris L, et al. Benchmarking challenging small variants with linked and long reads. Cell Genom. 2022;2(5):100128. doi:10.1016/j.xgen.2022.100128
- Wagner J, Olson ND, Harris L, et al. Curated variation benchmarks for challenging medically relevant autosomal genes. Nat Biotechnol. 2022;40(5):672-680. doi:10.1038/s41587-021-01158-1
- Illumina. イルミナゲノムの可能性を最大限に引き出す:DRAGENインフォマティクスと高品質のシーケンスにより、バリアントコールの質を高めるジャーニー。https://www.illumina.com/science/genomics-research/articles/CMRG_hg38.html アクセス日:2025年7月17日
- Ultima Genomics UG 100 Sequencing Platform specification sheet 2025年発表。アクセス日:2025年7月17日
- Fotsing SF, Margoliash J, Wang C, et al. The impact of short tandem repeat variation on gene expression. Nat Genet. 2019;51(11):1652-1659. doi:10.1038/s41588-019-0521-9
- Van Damme T, Pang X, Guillemyn B, et al. Biallelic B3GALT6 mutations cause spondylodysplastic Ehlers-Danlos syndrome. Hum Mol Genet. 2018;27(20):3475-3487. doi:10.1093/hmg/ddy234
- Grigsby J. The fragile X mental retardation 1 gene (FMR1): historical perspective, phenotypes, mechanism, pathology, and epidemiology. Clin Neuropsychol. 2016;30(6):815-833. doi:10.1080/13854046.2016.1184652
- Semmler L, Reiter-Brennan C, Klein A. BRCA1 and Breast Cancer: a Review of the Underlying Mechanisms Resulting in the Tissue-Specific Tumorigenesis in Mutation Carriers. J Breast Cancer. 2019;22(1):1-14. doi:10.4048/jbc.2019.22.e6
- Fu X, Tan W, Song Q, Pei H, Li J. BRCA1 and Breast Cancer: Molecular Mechanisms and Therapeutic Strategies. Front Cell Dev Biol. 2022;10:813457. 2022年3月1日発表。doi:10.3389/fcell.2022.813457
- Schulte J, Littleton JT. The biological function of the Huntingtin protein and its relevance to Huntington's Disease pathology. Curr Trends Neurol. 2011;5:65-78.
- Bishara J, Keens TG, Perez IA. The genetics of congenital central hypoventilation syndrome: clinical implications. Appl Clin Genet. 2018;11:135-144. 2018年11月15日発表。doi:10.2147/TACG.S140629
- Coffin SL, Durham MA, Nitschke L, et al. Disruption of the ATXN1-CIC complex reveals the role of additional nuclear ATXN1 interactors in spinocerebellar ataxia type 1. Neuron. 2023;111(4):481-492.e8. doi:10.1016/j.neuron.2022.11.016
- Goswami R, Bello AI, Bean J, et al. The Molecular Basis of Spinocerebellar Ataxia Type 7. Front Neurosci. 2022;16:818757. 2022年3月24日発表。doi:10.3389/fnins.2022.818757
- Leardini D, Messelodi D, Muratore E, et al. Role of CBL Mutations in Cancer and Non-Malignant Phenotype. Cancers (Basel). 2022;14(3):839. 2022年2月8日発行。doi:10.3390/cancers14030839
- Winnepenninckx B, Debacker K, Ramsay J, et al. CGG-repeat expansion in the DIP2B gene is associated with the fragile site FRA12A on chromosome 12q13.1. Am J Hum Genet. 2007;80(2):221-231. doi:10.1086/510800
- Barratt KS, Arkell RM. ZIC2 in Holoprosencephaly. Adv Exp Med Biol. 2018;1046:269-299. doi:10.1007/978-981-10-7311-3_14
- Malerba A, Klein P, Lu-Nguyen N, et al. Established PABPN1 intranuclear inclusions in OPMD muscle can be efficiently reversed by AAV-mediated knockdown and replacement of mutant expanded PABPN1. Hum Mol Genet. 2019;28(19):3301-3308. doi:10.1093/hmg/ddz167
- Tazelaar GHP, Dekker AM, van Vugt JJFA, et al. Association of NIPA1 repeat expansions with amyotrophic lateral sclerosis in a large international cohort. Neurobiol Aging. 2019;74:234.e9-234.e15. doi:10.1016/j.neurobiolaging.2018.09.012
- Bavassano C, Eigentler A, Stanika R, et al. Bicistronic CACNA1A Gene Expression in Neurons Derived from Spinocerebellar Ataxia Type 6 Patient-Induced Pluripotent Stem Cells. Stem Cells Dev. 2017;26(22):1612-1625. doi:10.1089/scd.2017.0085
- Deng J, Yu J, Li P, et al. Expansion of GGC Repeat in GIPC1 Is Associated with Oculopharyngodistal Myopathy. Am J Hum Genet. 2020;106(6):793-804. doi:10.1016/j.ajhg.2020.04.011
- van Kuilenburg ABP, Tarailo-Graovac M, Richmond PA, et al. Glutaminase Deficiency Caused by Short Tandem Repeat Expansion in GLS. N Engl J Med. 2019;380(15):1433-1441. doi:10.1056/NEJMoa1806627
- Kühnel T, Leitão E, Lunzer R, et al. Repeat Expansions with Small TTTCA Insertions in MARCHF6 Cause Familial Myoclonus without Epilepsy. Mov Disord. 2025;40(7):1401-1408. doi:10.1002/mds.30192
- Goodman FR、Bacchelli C、Brady AF、et al. Novel HOXA13 mutations and the phenotypic spectrum of hand-foot-genital syndrome. Am J Hum Genet. 2000;67(1):197-202. doi:10.1086/302961
- Kumutpongpanich T, Ogasawara M, Ozaki A, et al. Clinicopathologic Features of Oculopharyngodistal Myopathy With LRP12 CGG Repeat Expansions Compared With Other Oculopharyngodistal Myopathy Subtypes. JAMA Neurol. 2021;78(7):853-863. doi:10.1001/jamaneurol.2021.1509
- Yu H, Wu J, Cong J, et al. Congenital insensitivity to pain associated with PRDM12 mutation: Two case reports and a literature review. Front Genet. 2023;14:1139161. 2023年3月20日発行。doi:10.3389/fgene.2023.1139161