分子診断ラボにおけるNGS導入の変遷
はじめに
次世代シーケンサー(NGS)テクノロジーは、ヒトの疾患、特にがんに関与する変異に関連するバリアントの発見を加速させてきました。そういった研究での発見の中には、世界中の分子診断研究室で現在使われている、コンパニオン診断と薬事未承認検査法(LDT)の基礎になるものが出てきました。これらの研究室は現在、NGS腫瘍学検査の規制と保険料払い戻し戦略の発展の局面に直面しています。
シンガポールで開催された最近のイルミナユーザーグループ会議では、世界中の主要なオピニオンリーダーが、現在および将来の腫瘍学におけるNGS検査の影響に関するパネルディスカッションに参加しました。パネリストには以下が含まれていました。Lawrence Jennings, MD, PhD, Northwestern University Feinberg School of Medicine; Simon Patton, PhD, European Molecular Genetics Quality Network; Min-Han Tan, MBBS, PhD, Lucence Diagnostics; Benedict Yan, MBBS, National University Hospital Singapore。オーディエンスは、新しい政府検査基準からNGS検査頻度まで、さまざまな問題に焦点を当てた一連のポーリング質問を通じてパネルディスカッションに参加しました。1 ここでは、世界中の分子診断ラボでNGSの実施が直面する変化する状況と逆風に関する洞察をいくつか取り上げます。

左から右へ:Lawrence Jennings, MD, PhD, Attending Pathologist, Director, HLA and Molecular Diagnostic Laboratory, Northwestern University Feinberg School of Medicine; Simon Patton, PhD, Director, European Molecular Genetics Quality Network(EMQN); Min-Han Tan, MBBS, PhD, Founder and CEO, Lucence Diagnostics; Benedict Yan, MBBS, Pathologist, Head, Molecular Diagnostics Centre, National University Hospital.
Q:単一遺伝子検査をマルチ遺伝子NGSパネルに置き換える分子遺伝学ラボは、どのくらいの速さで見られますか?
Lawrence Jennings(LJ):調査から、ほとんどの回答者は将来、マルチ遺伝子NGSパネルに移行すると考えています。ラボでは、2つの理由から、単一検体検査から多検体NGSパネル検査に移行しています。第一に、1つのサンプルでマルチアナリティックテストを最終的に実施する必要があることを知っています。2つ目の理由は、NGSパネルテストのワークフローが、複数の単一分析物テストを実行するよりも簡単なためです。
Simon Patton(SP):NGSは技術であることを念頭に置く必要があります。重要なのは、実際に尋ねられている臨床的な質問です。NGSパネルを実施して臨床的な質問に答えることが適切でない場合、その理由は何ですか? その疾患に明確に存在する3つの定義された再発性変異の検査を行える場合、より広範なNGSパネルを使用する理由はありません。正しい答えを提供するために、正しいツール、または正しいテクニックを使うことです。
LJ:また、報告すべき内容の問題にもなります。臨床的有用性の観点から、ラボの臨床医は、BRAF、EGFR、NRAS、およびKRASのサンプル分析の臨床的関連性を認識する可能性があります。もちろん、同時に解析する方が簡単です。ポーリング結果(図1)の1つで見たように、腫瘍学者はより大きなパネルを要求しています。ラボがターゲットの50遺伝子パネルまたは包括的な170遺伝子パネルを実行する場合、どの遺伝子サブセットがレポートに含まれるのかという疑問が生じます。KRAS、NRAS、BRAF、およびEGFRの50の遺伝子またはより小さなサブセットについて報告していますか?
ミンハンタン(MHT):当社は複数の国で事業を展開しており、アジア、ヨーロッパ、アメリカにおける払い戻しの違いを理解することが重要です。アジアでは、支払いのほとんどは高価な診断や薬剤の自己負担となります。その結果、アジアの多くの地域では逐次検査が引き続き重要です。
しかし、このツールは臨床シナリオに適合しなければならないことに同意します。シーケンステストは、特定の状況でも理にかなっています。NGSパネルは、生検組織が入手しにくい場合や質が悪い場合に明確な利点をもたらします。何が、いつ、最も大きな臨床的利益をもたらすかが常に重要です。
Q:調査回答者は、がんパネル検査に関する懸念領域として、意義不明のバリアント(VUS)、コスト、結果の正確性、結果の解釈を選択しました(図2)。同意しますか?
MHT:がんパネルが生殖細胞系列検査用か体細胞検査用かによって異なります。生殖細胞系列検査の主な問題の1つはVUSで、臨床医のバックグラウンドスキルやトレーニングに応じて異なるアプローチを取ることができます。体細胞検査では、VUSはすぐに気になる問題ではありません。なぜなら、実行可能な変異の大部分は極めて明確だからです。
LJ:結果の解釈は、特にサプライズバリアントがある場合、問題になる可能性があります。ディスカッションでは、このバリアントが存在することがわかった今、どのような行動が取られるのかという話になります。
SP:私の習熟度テスト(PT)スキームでは、精度が問題であることに気づきました。特に腫瘍学や、テストの開発と実装の新たな分野では、多くのエラーが見られます。ジェノタイピングの平均エラー率は3%弱です。新しい腫瘍学検査の多くが実施されたとき、エラー率は約25%でした。そのため、4分の1の検査結果が間違っていました。驚くべきことに、これは外部品質保証(EQA)スキームの結果であり、ラボはこれがEQAサンプルであることを知っていました。臨床シナリオにおける真の根底にあるエラーは何ですか? 25%未満ですが、予想以上に高くなっています。

図 1:投票結果–腫瘍学者が要求する検査の複雑さのレベルは?1
Q:どのテストを実行するかを決定する際、報告義務のある結果あたりのコストはどの程度影響しますか?
MHT:NGSパネルの費用は、医療システムと償還アプローチによって異なります。一部の米国の医療システムでは、NGSパネルがカバーされています。アジアでは、NGSパネルのほとんどが自己負担です。肺がんでは、NGSパネルは、回答までの全体的な時間を短縮し、またはリキッドバイオプシーが患者の処置を無駄にし、コストを削減することで、コストを削減することができます。NGSパネルのバリデーションが時間とともに改善し、FDAやCFDAがより多くの提出書類を審査するにつれて、明確な臨床的利点を考慮してNGSパネルへのアクセスが増えます。
Ben Yan(BY):コストは間違いなく私たちの関心事です。最近の米ドル増はシンガポールの試薬コストに影響を与え、患者1人あたりのコストを50シンガポールドル増加させました。
LJ:私の視点では、この価値ははるかに重要です。コストは、市場が許容する内容に応じて試薬コストを設定するベンダーによって主に決定されます。これは、この検査がもたらす価値、さらには競合他社の試薬の払い戻しとコストを反映しています。同じ価値の2つのテストを考えると、コストが要因になります。プラットフォームやワークフローの標準化などのその他の要因も関与します。
Q:また、参加者は、がん患者が診断時、再発時、非標的療法の選択肢がなくなる時、またはまったくない時に、がんサンプルをシーケンスすべき時期に関する多肢選択式の質問にも回答しました(図3)。診断、再発、および非ターゲット療法の選択肢がなくなると均等に分けられました。同意しますか?
LJ:固形腫瘍の場合、診断と再発のために、3つのすべての事例でシーケンスを実施することは理にかなっていると思います。
署名:血液がんの場合、白血病が根絶された後、患者が再発する前にシーケンスを行うことが良い考えです。シーケンスにより、どのような変異がまだ存在するかがわかる可能性があります。
LJ:移植後、または患者が寛解中の場合に、骨髄検査用のNGSパネルを注文する臨床医がいます。ほとんどのNGSパネルは診断用に設計されており、検出限界は5%です。移植後および寛解検査には、微小残存病変(MRD)に関連するバリアントをターゲットにしたパネルが必要です。診断に使用される検査の多くはMRD検査ではありません。MRD検査では、パネルの検出限界が0.1%以上である必要があることを認識することが重要です。
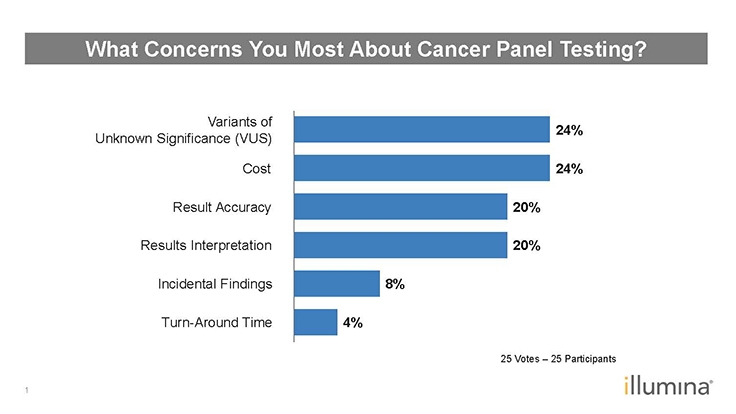
図 2:投票結果 – がんパネル検査について最も懸念する点1
Q:現在、腫瘍変異負荷(TMB)検査は完全には予測できず、TMB検査によって異なる結果が得られます。TMBテストに関するEQAの見解はどのようなものですか?
SP:TMBのEQAを開発する予定です。おっしゃった理由から、ラボのパフォーマンスとTMBの解釈を理解するために調査を実施しています。TMB-highとTMB-lowの結果は不明ですか? 10は任意のカットオフポイントですか? TMBは1つの臨床試験、または2つのTMBテストの比率に基づいて決定されますか?
当社はInternational Quality Network for Pathology(IQN Path)と協力して、TMBテスト用のEQAの開発の範囲を定めています。ラボはTMBの測定方法に苦労しており、臨床医はTMBテストデータの解釈方法に苦労しているため、この状況はすぐには起こりません。
Q:NGS腫瘍学パネルの臨床的妥当性、有用性、費用対効果のエビデンスを作成するために、コミュニティとして何ができますか?
MHT:当社は、公的および民間の利害関係者、および国際的なEQA機関が集結し、質の高い結果を達成し、患者のコストを削減するグローバルコミュニティです。研究者主導試験(IIT)、製薬主導試験、または政府支援の研究により、臨床的妥当性と有用性に関するデータを得ることができます。しかし、費用対効果の問題は困難です。これは、地域によって異なる払い戻し状況によって異なる場合があります。通常、すべての地域が独自の費用対効果分析を行います。費用対効果解析の分野でよく知られている英国NICEの優れた解析は、文脈を考慮して他の国でも引き続き評価されます。
LJ:すべては正確なデータにまで及びます。臨床的妥当性を得るには分析的妥当性が必要であり、臨床的有用性を得るには臨床的妥当性が必要です。しかし、まだ、解析の妥当性であるNGSデータには、臨床の妥当性について自信を持てるほどの自信はありません。
生殖細胞系列バリアントコミュニティにはClinVarデータベースがあり、急速に成長し、臨床的妥当性の定義に有用になっています。以前は、Human Gene Mutation Database(HGMD)を持っていました。HGMDは、マニュアルでキュレーションされた、文献中のバリアントコールのデータベースでした。残念なことに、HGMDのコールの約3分の2はオーバーコールであったため、データベースは役に立ちませんでした。これとは対照的に、ラボでは、疾患関連バリアントと表現型の関係に関するデータを含むレポートをClinVarにアップロードします。クエリが容易な無料アーカイブで、有用な、よくアノテーションされた、よく分類されたバリアント情報で構成されています。
体細胞バリアントコミュニティが同様のデータベースを作成することは可能だと思います。cBioPortalとOncoKBデータベースでは、ある程度この傾向が見られます。課題は、データをインポートするための標準構造を作成することです。
SP:臨床バリデーションでは、データ標準と命名法の調和が必要です。これは、どの表現型のどのバリアントについて同じことを話しているかを確認するために必要です。これまでお話ししてきたデータベースは、それ以外には機能しません。
ベストプラクティスのガイドラインを書くことは、組織として非常に強く感じていることです。当社は、患者のために最善を尽くし、正しい結果を得ようとしているラボのコミュニティです。NGSパネルの実装において、ラボのガイダンスを改善するために協力する必要があります。
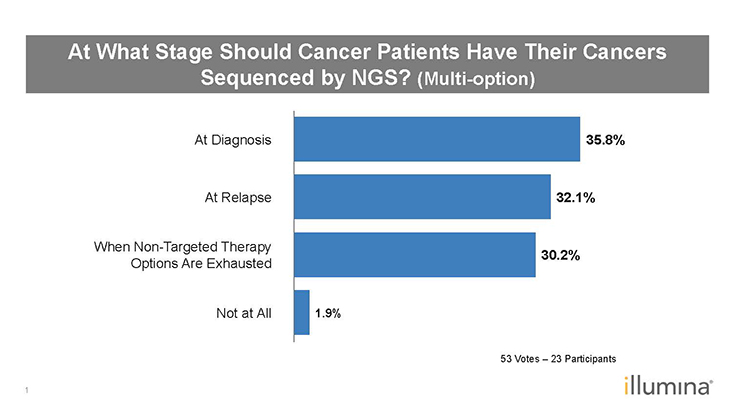
図 3:投票結果 – がん患者はどの段階でNGSのシーケンスを受けるべきでしょうか? 1
Q:専門のリファレンスセンター外でのNGSの幅広い導入をサポートするには、どのような変更が必要ですか?
MHT:主流の市場テストの重要な側面の1つは、かかりつけ医レベルです。米国では、Regeneron Genetics CenterとGeisinger Health Systemが協力して、よく理解された予防可能な疾患に焦点を当てたエクソームシーケンスに250,000人を登録することを目標としています。2目標は、年間100,000エクソームのシーケンスと解析です。ある意味では、科学の幸運を語る領域に進出しています。その情報の意味は、臨床医の教育の必要性とともに進化しています。私たちは必ずしもこれをうまく行うわけではありません。実際、米国のような資源の豊富な国では、BRCA検査の3分の2が遺伝カウンセリングなしで実施されることが、論文で示されています。医療コミュニティとして、人々が結果を正しく理解し解釈するようにするにはどうすればよいでしょうか? この取り組みは、臨床および患者コミュニティが疾患予防に関する適切な会話を行えるように十分な教育を受けられるようにすることに焦点を合わせたべきではないでしょうか? Geisinger Health Systemは、エンベロープを押し上げ、人々との話し合いを促進するための基盤を作る上で正しいことをしています。
SP:遺伝学はさらに主流になります。過去10年間のNGSの成長を見てください。この5~6年で腫瘍学領域だけが劇的に成長しました。患者のベッドサイドで遺伝学検査を実施することで、ポイントオブケア検査の大幅な増加を予測しています。これらの迅速検査は、より迅速な患者ケアの意思決定プロセスに役立つ可能性があります。遺伝学が主流の医学の一部になるにつれ、特に一般開業医のために臨床医の教育をより多く見る必要があります。一般開業医(GP)はすでに遺伝子検査のオーダープロセスに関与しています。
LJ:消費者直送とベッドサイドの遺伝子検査は共通して同じであり、患者とその家族が検査結果を理解できるように遺伝カウンセリングの必要性があります。例えば、生殖細胞系列検査を実施し、ホモ接合型第V因子ライデンを同定した場合、中年女性喫煙者である兄弟姉妹に与える影響ほど、患者に与える影響はそれほど大きくない可能性があります。検査を行い、このバリアントを同定し、他の家族にそのバリアントを所有している可能性があること、および健康への影響について知らせることはできていませんか? 誰かがBRCA検査を受けた場合、残りの家族に知らせる義務がありますか? 体細胞バリアントであっても、生殖細胞系列バリアントを調べており、偶発的な所見があるかもしれません。
課題は、これらのシナリオについて家族や患者に助言するための遺伝カウンセリングリソースがないことです。プライマリーケア医師、医師助手(PA)、看護師登録(RN)、および高度医療看護師(APN)の間で、プライマリーケア面に関する教育がさらに必要です。
SP:BRCA検査は、体細胞と生殖細胞系列の視点を交配させた最初の主流遺伝子検査であるため、このパラダイムはすでに存在します。臨床診療の面では懸念です。この種の検査の臨床実施には多くのバリエーションがあり、教育は非常に重要です。体細胞変異検査を行うだけで生殖細胞系列について完全に忘れてしまうラボが数多くあり、そのため変異を見つけることの家族的意味合いがわかります。
LJ:例えば、小児科では、がんを持つ子供の約10~15%に生殖細胞系列の素因バリアントがあります。これは家族全員にとって意味があります。検討せずに、単に子供に遺伝子検査を実施することはできません。
まとめ
NGSは、世界中の分子診断ラボで不可欠なツールであり、今後その存在になる予定です。臨床医と病理学者は、患者の診断と治療における単一および多検体NGSがんパネル検査によってもたらされる潜在的な価値と利点を理解しています。NGSパネルが世界中でルーチンの臨床試験となる前に、臨床的妥当性を確保するための分析的妥当性データ、堅牢な臨床バリアントデータベース、NGSパネル検査の償還戦略、およびベストプラクティスガイドラインが必要です。
続きを読むことに興味がありますか?
2019年1月、イルミナは、FDAが汎がんアッセイの優先審査とリソースを付与したことを発表しました。
イルミナの新しいリキッドバイオプシーとハイスループットアッセイについては、こちらをご覧ください。
参考文献
- 参加者のポーリング応答データ。プレシジョンオンコロジーミーティングでのNGSの実施。シンガポール。2018年8月17日
- Regeneron。Regeneron Genetics CenterとGeisinger Health System Collaborationについて。www.regeneron.com/sites/all/themes/regeneron_corporate/files/science/RGC_FactSheet_GHSCollaboration_Final.pdf. 2018年10月15日にアクセス。
