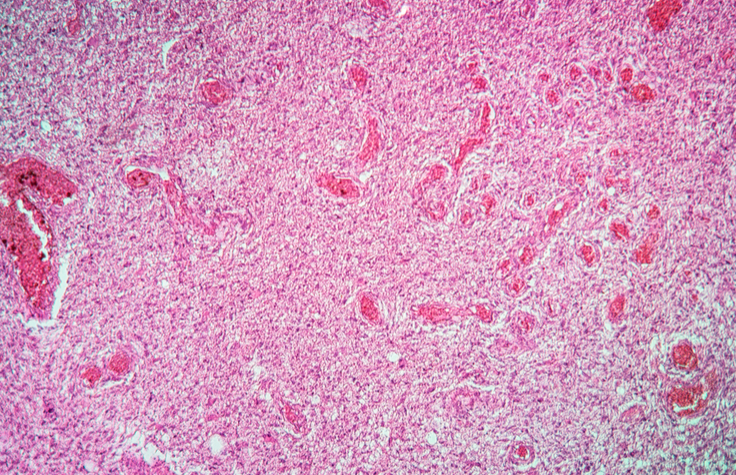
脳腫瘍研究で注目されたNGSパネル
はじめに
1885年に設立されたYonsei University College of Medicine Severance Hospitalは、韓国最大の大学病院の1つに成長しました。医療現場の最前線にあり、北東アジアの医療ハブになることに重点を置いています。病院の臨床医は現在、年間1,200を超える臨床試験を実施しています。また、その病理学チームは、疾患を同定し層別化するための臨床研究に次世代シーケンサー(NGS)を使用する方法もリードしています。
Se Hoon Kim医学博士は、退職者病院の病理学科の教授です。神経病理学を専門とし、神経膠腫などの脳腫瘍の信頼できる迅速で有益な診断のための新しいツールの評価を行っています。神経膠腫は、全脳腫瘍および脊髄腫瘍の約30%、全悪性脳腫瘍の80%を占めます。1イソクエン酸デヒドロゲナーゼ(IDH)1および2における変異は、低悪性度および二次性高悪性度神経膠腫において最も頻度の高い変異の1つです。2IDH変異の検出と同定は、神経膠腫患者の臨床ケアと予後において重要です。IDH1およびIDH2変異腫瘍を有する患者は、野生型IDH神経膠腫を有する患者と比較して生存期間が延長します。3 IDH1神経膠腫は侵襲性が低いものの、治療抵抗性があります。
Kiyong Na医学博士は、Division Fellowとともに、既存のゴールドスタンダード手法とNextSeq−(* 550システムでのTruSight Tumor 170アッセイとの比較研究を実施し、神経膠腫生検におけるIDH変異やその他のがん関連バリアントを検出しました。IDH変異を検出するための現在のツールには、免疫組織化学(IHC)やパイロシーケンスが含まれます。TruSight Tumor 170は、DNAとRNAの解析をサポートするターゲットパネルで、固形腫瘍に関連する幅広い遺伝子とバリアントを網羅しています。NGSデータは、これらの現在のアプローチと比較して良好でした。iCommunityは、Kim博士とNa博士に、彼らの研究と、NGSが将来の腫瘍の特性評価と診断において果たす役割について話しました。

Se Hoon Kim医学博士は病理学の教授であり、Kiyong Na医学博士は韓国ソウルの退職者病院の部門フェローです。
Q:脳腫瘍を評価するためのテクノロジー評価研究の焦点は何ですか?
Se Hoon Kim(SHK):当社は、スピードと信頼性、およびそれらが提供する情報が神経病理学検体中の既知の遺伝子マーカーの同定に臨床的に有用であるかどうかを判断するために、新しいテクノロジーを評価しています。当社の病理検査室では現在、qPCR、サンガーシーケンス、蛍光in situハイブリダイゼーション(FISH)を使用して腫瘍生検サンプルを評価しています。世界中の企業や研究機関が、新しい解析技術を継続的に開発しています。相関研究を行い、当社の標準的な手順と比較して、これらの新しいアプローチの精度、信頼性、費用対効果、および潜在的なターンアラウンドタイムを決定します。
Q:脳の研究でTruSight Tumor 170とNextSeq 550システムを使い始めたのはいつですか?
キヨンナ(KN):2017年に韓国政府がNGSベースの検査の選択的な払い戻しを申し出た際、NextSeq 550システムの使用を開始しました。
SHK:新しい変異を同定するための研究を実施するのではなく、NGSベースの検査を使用して、診断や個別化治療に有望なマーカーを同定または確認しています。
KN:例えば、TruSight Tumor 170 BRAF変異データを用いて腫瘍サンプルのサブタイプを再評価しました。別の症例では、TruSight Tumor 170データを用いてヘテロ接合性喪失(LOH)評価を再評価することができました。
また、NextSeq 550システムを使用して、神経膠芽細胞腫で過剰発現する融合バリアント、上皮細胞増殖因子受容体(EGFR)増幅、およびEGFRvIII変異を検出します。以前は、EGFR増幅を検出するためにFISHを使用しました。TruSight Tumor 170とNextSeq 550システムを使用して、EGFR増幅の検出は世界的に報告された傾向と一致しています。
Q:TruSight Tumor 170 PanelとNextSeq 550システムを用いた神経膠腫生検サンプル研究のパラメーターは何ですか?
SHK:NextSeq 550システムのTruSight Tumor 170と、びまん性神経膠腫として知られる特定の脳腫瘍サブセットにおける臨床的に意義のある遺伝子変異を評価するために使用したその他の分子診断法との比較研究を実施しました。びまん性神経膠腫は、成人で最もよく見られる脳腫瘍であり、神経垢に腫瘍細胞がびまん性に浸潤することを特徴とします。これは、神経細胞とグリア細胞のプロセスの密なネットワークです。
KN:過去1年間に受領したびまん性神経膠腫サンプルをすべて採取しました。NextSeq 550システムで200を超えるサンプルをTruSight Tumor 170で再解析し、そのバリアント検出性能を標準手法と比較しました。
表1:びまん性神経膠腫サンプルのIHC、パイロシーケンス、NGS解析の比較研究データ。
遺伝子/バリアント/アッセイ |
コンパレータアッセイ |
次世代シーケンサー(NGS) |
|||||
|---|---|---|---|---|---|---|---|
IDH1 IHC |
135 |
R132H |
その他の変異体 |
ワイルドタイプ |
一致率 |
||
R132H変異体 |
38 |
38 |
0 |
0 |
100% |
||
| R132H野生型 | 97 |
0 |
0 |
97 |
100% |
||
BRAF IHC |
17 |
V600E |
その他の変異体 |
ワイルドタイプ |
一致率 |
||
VE1変異体 |
5 |
5 |
0 |
0 |
100% |
||
VE1野生型 |
12 |
0 |
1 |
11 |
100% |
||
IDHパイロシーケンス |
48 |
IDH1変異体 |
IDH2変異体 |
ワイルドタイプ |
一致率 |
||
| IDH1変異体 | 0 |
0 |
0 |
0 |
100% |
||
| IDH1野生型 | 48 |
|
0 |
0 |
48 |
100% |
|
| IDH2変異体 | 0 |
0 |
0 |
0 |
100% |
||
| IDH2野生型 | 48 |
0 |
0 |
48 |
100% |
||
TERTパイロシーケンス |
135 |
TERT変異体 |
その他の変異体 |
結果なし |
一致率 |
||
C228T変異体 |
53 |
53 |
0 |
0 |
100% |
||
C250T変異体 |
17 |
17 |
0 |
0 |
100% |
||
野生型 |
65 |
0 |
3 |
62 |
100% |
||
Q:びまん性神経膠腫サンプルを用いたこの比較試験の結果はどうでしたか?
KN:私たちの研究で最も重要なターゲット遺伝子はIDHでした。以前は、IHCまたはピロシーケンスを使用して、採取中のびまん性神経膠腫サンプルを解析していました。TruSight Tumor 170は、以前の解析アプローチと100%一致したIDHバリアントの有無を正常に報告しました(表1)。検出されたIDH変異はすべてR132Hにあり、これは脳腫瘍で最もよく見られるIDH変異であることが知られています。TruSight Tumor 170は、最も一般的なIDH変異を安定して検出することが奨励されています。さらに、TruSight Tumor 170は、免疫化学法で見られたTPTP53およびBRAF変異レベルと同様のレベルを同定しました。
また、TERTプロモーター変異ステータスのパイロシーケンスとNGSデータも比較しました。C228TおよびC250Tバリアントは、TERTプロモーター領域の最も一般的なバリアントです。TruSight Tumor 170データは、従来のパイロシーケンスと相関性が高く、パイロシーケンスデータに含まれていないいくつかの小さなバリアントも検出しました。TERTプロモーター変異の検出は、びまん性神経膠腫に不可欠です。しかし、TETプロモーター領域のC228Tバリアントは、リード深度が最適ではないため、*.vcfファイルで除外されることがよく見られました。その結果、このゲノム領域のバリアントについて、Integrated Genome Viewer(IGV)を詳しく調べる必要がありました。この領域のカバレッジが最適でない原因を突き止めることに熱心でした。また、他のNGSでも、TERTプロモーター領域のリード深度が低いことが報告されました。panels.It。
興味深い所見の1つは、1p/19qコードレットに関するものです。TruSight Tumor 170では、NRAS11、MYCL11(1p)、CCNE11、AKT2、ERCC11、ERCC2(19q)などの1p遺伝子と19q遺伝子の大幅なコピー数減少がオリゴデンドロ神経膠腫のほとんどに認められました。これは、乏突起神経膠腫サンプルにおけるFISHデータと良好な相関関係を示しました。データから、このクラスター化されたコピー数の減少は、1pおよび19q遺伝子の欠失を反映している可能性があることが示唆されています。TruSight Tumor 170が1pおよび/または19q領域内に位置するより多くの遺伝子を含む場合、このデータはより意味のあるものであったと考えられます。
" TruSight Tumor 170は、最も一般的なIDH変異を安定的に検出し、免疫化学法で見られるものと同様のTP53およびBRAF変異レベルを検出したと考えられます。"
Q:より広範なTruSight Oncology 500パネルは、TruSight Tumor 170パネルで発見したいくつかの問題をどのようにして解決しますか?
SHK:TruSight Tumor 170はフォーカスパネルです。その結果、脳腫瘍の評価に必要な包括的な遺伝子プロファイリングの実施にはいくつかの限界があります。
これらの問題は、500を超える遺伝子を網羅する汎がんパネルであるTruSight Oncology 500パネルの導入により、すでに解決されていると考えています。TruSight Tumor 170よりも包括的で、一塩基バリアント(SNV)、インデル、増幅、融合、スプライスバリアントなど、さまざまなタイプのバイオマーカーを同時に解析できます。また、腫瘍変異負荷(TMB)とマイクロサテライト不確かさ(MSI)の状態も測定します。これは将来の免疫腫瘍学治療をサポートする上で不可欠なバイオマーカーです。4
Q:研究でTruSight Tumor 170データをどのように解析しましたか?
KN:TruSight Tumor 170データの解析は、*.vcfファイルに基づいています。Yonsei病理学の他のメンバーと社内でいくつかのろ過基準を設定しました。バリアントの最終選択は、内部ろ過および選択標準を使用して手動で行われます。
場合によっては、一塩基欠失と重複の間のバリアントコールアルゴリズムの混乱により、バリアントコールが標準的な命名法から外れる可能性があることがわかりました。これは、韓国の1000ゲノムプロジェクトからのデータをデータろ過プロセスに組み入れるか、データを通常の参照データとして使用することで解決できる可能性があります。これにより、韓国のサンプルにおける体細胞バリアントコールの精度が大幅に向上します。
Q:NGSとメチル化アレイを組み合わせて脳がんサンプルを評価する価値はありますか?
SHK:NGSを用いた体細胞変異プロファイリングは、臨床診療で日常的に行われるようになると思います。また、脳腫瘍の包括的な遺伝子プロファイリングは、メチル化アレイ解析の恩恵を受けると考えています。これは、ドイツがん研究センター(DKFZ)におけるDavid Capper博士のプロジェクトで、脳腫瘍サンプルのメチル化解析にInfinium #@ HumanMethylation450KおよびMethylationEPICアレイを使用して示されています。5
韓国で私たちが抱えている問題は、メチル化アレイはここではまだ払い戻しを受けておらず、脳がんの変異の同定における使用を調査する臨床研究を実施するために得られる資金が制限されていることです。また、国際的な協力関係を支援するために必要な場合、臨床/遺伝学データを国際的に輸送または共有する規制上の問題もあります。
"新しいTruSight Oncology 500パネルは、より包括的で、さまざまなタイプのバイオマーカーを同時に解析できるものです。"
Q:韓国におけるNGS遺伝子評価の規制と払い戻しはどのように進化していますか?
SHK:韓国政府の当初の発表によると、NGSベースの臨床試験の選択的償還プログラムについて、2018年後半にレビュープロセスが実施されます。この問題は、脳腫瘍患者や家族の間で韓国で注目を集めています。患者支援団体は、NGSなどのハイテク診断検査や新しい脳腫瘍薬への個人アクセスを強く求めています。これらは現在、韓国政府が規制する公的医療支援制度では提供されていません。
Q:NGSの民主化はあなたにとってどのような意味がありますか?
SHK:民主化は、平均的な患者の利益のために、NGSへの普遍的かつ一般的なアクセスを提供するという意味であれば、前向きな側面があると思います。包括的なNGSデータにアクセスし、NGS解析テクノロジーを簡単に利用できるようにすることで、ベンチとベッドサイドのギャップを埋めることができます。
しかし、私は、世界中でハイテク医療ツールが利用できることを懸念しています。NGSやその他のハイテク医療ツールの利用可能性に現在のギャップがあることから、今後、異なる経済学クラス間、および未開発の国と富裕国の間で、より広くなる可能性があります。同じことが、新しい、しかし高価な治療法や薬剤が利用できることで起こる可能性があります。私は、NGSベースのツール、診断、および治療法の可用性と品質における、さまざまな社会的クラスや国におけるギャップの拡大や偏りを、どのように制限するかを懸念しています。
Q:NGSと腫瘍学の次の展望は何だと思いますか?
SHK:臨床現場でのNGS技術の受け入れは、今後避けられないでしょう。優れた例はPCRの受け入れです。20年前、PCRは臨床診療において不可欠なテクノロジーになるとは思いませんでした。しかし、それにはあります。NGSテクノロジーでも同じことが起こります。すでに、当院での臨床研究用サンプルのNGS解析の実施依頼が急増しています。
Q:今後、どのようなタイプのNGSがんパネルを使用する予定ですか?
KN:新しいTruSight Oncology 500パネルは、より包括的で、さまざまなタイプのバイオマーカーを同時に解析できるものです。新しい治療法のコンパニオン診断薬の開発の基礎として理想的です。韓国でこのパネルをテストし、検証する機会が間もなく得られるのを楽しみにしています。
また、固形腫瘍を固形腫瘍クラスIまたはIIのパネルなど、いくつかのクラスに分類するために必要な遺伝子で作成された新しいNGSパネルもご覧になりたいと考えています。脳がんの臨床的に重要なターゲット遺伝子を持つ新しいパネルも、当社の臨床研究に役立つでしょう。
この記事で言及されている製品とシステムの詳細はこちら:
Infinium MethylationEPIC BeadChipキット
参考文献
- Goodenberger MLおよびJenkins RB。成人神経膠腫の遺伝学 がん遺伝子。2012年、205年:613~621。
- 神経膠腫におけるCohen A、Holmen S、およびColman H. IDH1およびIDH2変異。Curr Neurol Neurosci Rep . 2013; 13:345。
- Garrett M, Sperry J, Braas D, et al. イソクエン酸デヒドロゲナーゼ(IDH)変異およびIDH野生型グリオーマ球の代謝特性解析により、細胞型に特異的な脆弱性が明らかになります。 がんメタブ 2018. 6:4 doi: 10.1186/s40170-018-0177-4。
- Buchhalter I, Rempel E, Endris V, et al. サイズの重要性:パネルベースの腫瘍遺伝子変異量(TMB)解析のための重要なパラメーターの解析。Int J Cancer . 2018年。doi:10.1002/ijc.31878。
- Hench J, Bihl M, Bratic Hench I, et al. 神経腫瘍専門医の満足:日常的な分子神経膠腫診断への迅速なアプローチ。Neuro Oncol。2018. 12: 1682~1683。