CRISPRゲノム編集におけるNGS
CRISPRゲノム編集テクノロジー
CRISPR(Clustered Regularly Interspaced Short Palindromic Repeats)ゲノム編集は、プログラム可能なRNAがヌクレアーゼ(例: Cas9)をゲノムの特定の場所にターゲティングする革新的な方法です。1,2 CRISPR-Cas9テクノロジーは、遺伝子要素の変異、サイレンシング、誘導、または置換を高いスピード、シンプルさ、および精度で実現するため、世界中の研究コミュニティーで広く採用されています。
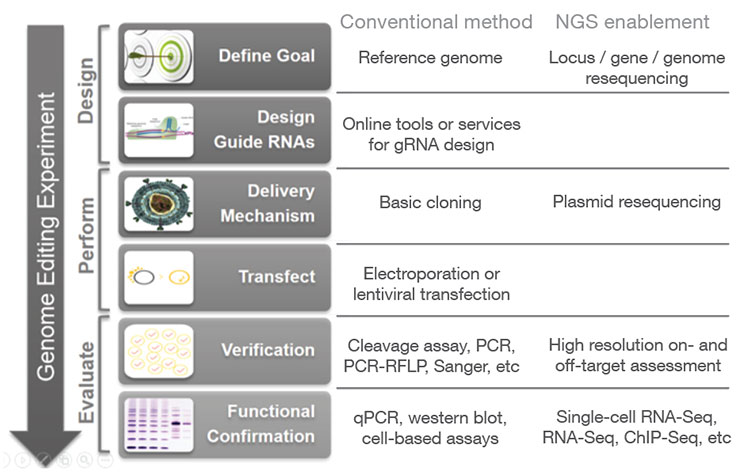
次世代シーケンス(NGS)は、全ゲノムシーケンスによるCRISPRオフターゲット効果の解析から、ターゲットシーケンスによるCRISPRノックアウトやその他の編集の確認まで、ゲノム編集ワークフローのさまざまな段階で使用可能です。その後、メチル化解析やRNAシーケンスによる遺伝子発現プロファイリングなどのアプリケーションを用いてフォローアップ研究を行い、特定の遺伝子編集の機能的影響を評価することができます。
CRISPRゲノム編集の応用
CRISPR-Cas9テクノロジーの応用は、基礎研究、臨床研究、治療、医薬品開発、農業、環境の分野で確認されています。臨床研究では、鎌状赤血球症、がん、AIDS、ハンチントン病、デュシェンヌ型筋ジストロフィーなどの疾患におけるCRISPRの活用の可能性が示唆されています。
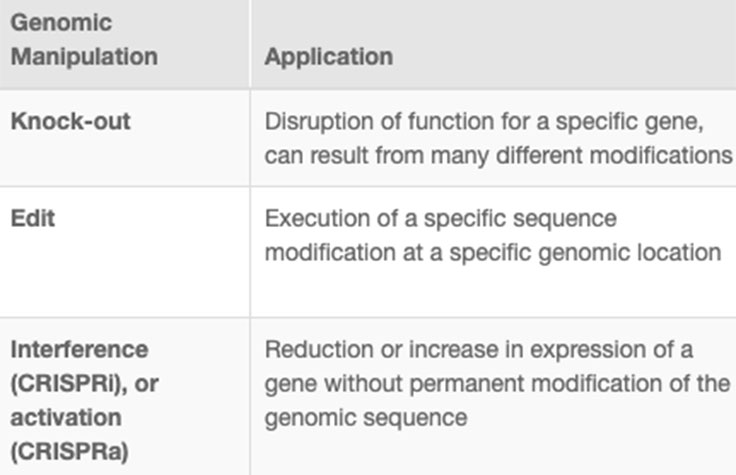
CRISPRゲノム編集により、研究者は遺伝子改変された細胞株や動物モデルを迅速かつ正確に作成することができます。遺伝子ノックアウトや遺伝子ノックインの作成に加えて、研究者はCRISPRテクノロジーを用いて、ゲノム配列を変更することなく、干渉(CRISPRi)または活性化(CRISPRa)を介して遺伝子発現を調節することができます。詳細については、関連する表を参照してください。
CRISPRノックアウトおよびその他の編集を確認する
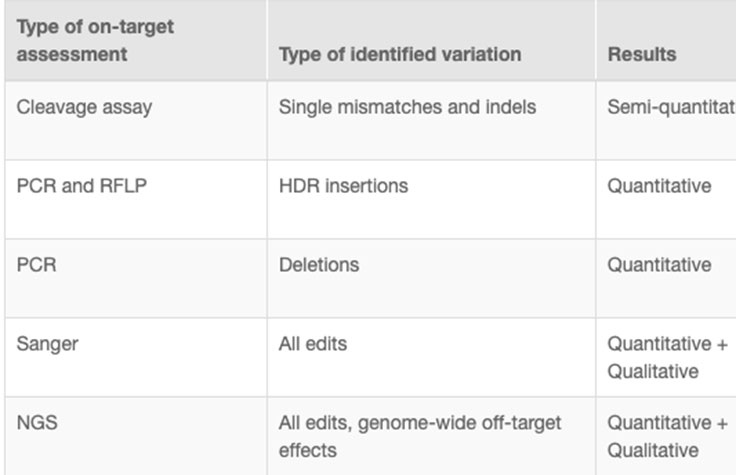
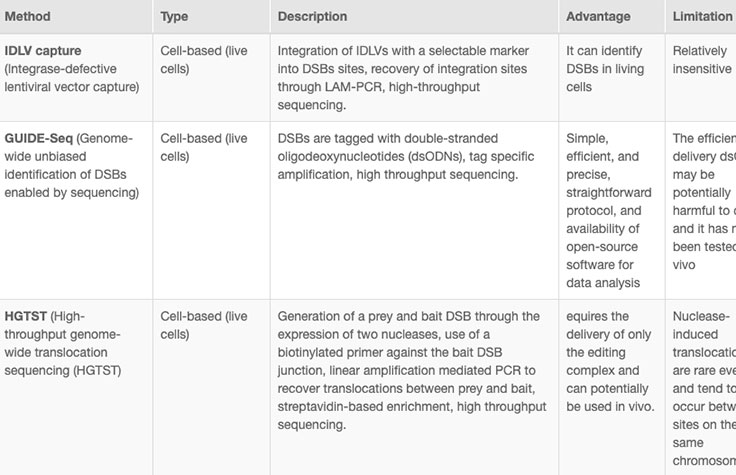
CRISPR ゲノム編集実験の結果として、混合細胞集団が生成され、目的の編集が行われるのは小さなサブセットのみになります。研究者は、どの細胞に望ましいCRISPRノックアウトまたは標的の変異があるかを判断する必要があります。編集を評価する現在の方法には、切断アッセイ、PCR、サンガーシーケンス、NGSなどがあります。追加情報については、関連する表を参照してください。
NGSは、あらゆる改変範囲にわたって定性的および定量的情報を高解像度で提供し、あらゆるスループットのニーズを満たし、オフターゲット効果をモニタリングするために使用できる唯一のアッセイです。7 NGSベースのターゲットシーケンスは、修正対象領域に焦点を当てることでCRISPR誘導編集を確認するコスト効率の高いソリューションを提供します。
ターゲットシーケンスの詳細はこちらNGSを用いたCRISPRオフターゲット解析
CRISP/Cas9技術の実施を成功させるには、目的のターゲット以外の部位における意図しない改変であるオフターゲット効果を特定し、低減するストラテジーなどが必要となります。ゲノム編集実験では、RNAの特異性を評価し、オフターゲット部位を予測する計算法が広く使用されています。
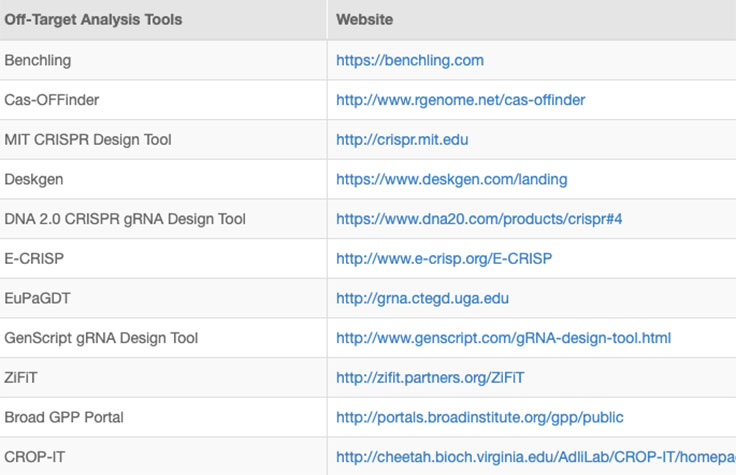
オンラインツールやウェブベースのアルゴリズムが公開されています(表)。ただし、予測アルゴリズムでは見逃されるおそれのあるオフターゲット部位を発見するには、NGSによる全ゲノムシーケンス(WGS)などの全ゲノム解析が必要です。8
WGSの詳細はこちら注目のCRISPR-Cas9ゲノム編集に関するコンテンツ
CRISPR-Cas9:ゲノムエンジニアリングをシンプルに
イルミナのサイエンティフィックアフェアーズチームは、CRISPR-Cas9テクノロジーの応用に関する主要な出版物をまとめています。
動画を視聴
長鎖ノンコーディングRNAとがん
研究者は、バイオマーカーの発見からがん特異的lncRNAをサイレンシングするためのCRISPRベースおよびsiRNAベースのアプローチまで、最近のがん関連lncRNA研究について考察しています。
インタビューはこちらCRISPRゲノム編集の機能的影響に対する評価
サイエンティストは、編集された配列が遺伝子の構造と機能に与える影響を判断するために、さまざまな配列解析手法を使用することができます。遺伝子編集の機能的影響を研究するために一般的に使用される方法には、以下のようなものがあります。
Single-Cell RNA-Seq
CRISPR修飾後に細胞集団をスクリーニングし、数千個の個々の細胞において、多くの遺伝子の制御への影響を並行して判定します。
RNAシーケンス
トランスクリプトーム全体または遺伝子/遺伝子ファミリーの発現に対する変異の影響を評価します。
クロマチン免疫沈降シーケンス(ChIP-Seq)
DNA-タンパク質結合に対するゲノム編集の影響を評価します。
メチル化シーケンシング
メチル化状態とクロマチンリモデリングに対する変異の下流への影響を評価します。
主な製品
Francis deSouzaによるゲノミクス、CRISPR、未来
Illumina, Inc.の社長兼CEOであるFrancis deSouzaは、コロラド州で開催されたAspen Ideas: Healthに登壇し、ゲノミクスが医療全体に及ぼしている影響と、その恩恵をより多くの人々により迅速にもたらす緊急性について、聴衆に向けて解説しました。
記事を読む
参考文献
- Cong L, Ran F A, Cox D, et al.Multiplex genome engineering using CRISPR/Cas systems.Science.2013;339:819-823.
- Mali P, Yang L, Esvelt KM, et al.RNA-guided human genome engineering via Cas9.Science.2013;339:823-826.
- Maruyama T, Dougan SK, Truttmann MC, Bilate AM, Ingram JR, Ploegh HL.Increasing the efficiency of precise genome editing with CRISPR-Cas9 by inhibition of nonhomologous end joining.Nat Biotechnol.2015;33:538-542.
- Chu VT, Weber T, Wefers B, et al.Increasing the efficiency of homology-directed repair for CRISPR-Cas9-induced precise gene editing in mammalian cells.Nat Biotechnol.2015;33:543-548.
- Qi LS, Larson MH, Gilbert LA, et al.Repurposing CRISPR as an RNA-guided platform for sequence-specific control of gene expression.Cell.2013;152:1173-1183.
- Cheng AW, Wang H, Yang H, et al.Multiplexed activation of endogenous genes by CRISPR-on, an RNA-guided transcriptional activator system.Cell Res.2013;23:1163-1171.
- Ran FA, Hsu PD, Wright J, Agarwala V, Scott DA, Zhang F. Genome engineering using the CRISPR-Cas9 system.Nat Protoc.2013;8:2281-2308.
- Tsai SQ, Joung JK.Defining and improving the genome-wide specificities of CRISPR-Cas9 nucleases.Nat Rev Genet.2016;17:300-312.
- Gabriel R, Lombardo A, Arens A, et al.An unbiased genome-wide analysis of zinc-finger nuclease specificity.Nat Biotechnol.2011;29:816-823.
- Tsai SQ, Zheng Z, Nguyen NT, et al.GUIDE-seq enables genome-wide profiling of off-target cleavage by CRISPR-Cas nucleases.Nat Biotechnol.2015;33:187-197.
- Chiarle R, Zhang Y, Frock RL, et al.Genome-wide translocation sequencing reveals mechanisms of chromosome breaks and rearrangements in B cells.Cell.2011;147:107-119.
- Crosetto N, Mitra A, Silva MJ, et al.Nucleotide-resolution DNA double-strand break mapping by next-generation sequencing.Nat Methods.2013;10:361-365.
- Kim D, Kim S, Kim S, Park J, Kim JS.Genome-wide target specificities of CRISPR-Cas9 nucleases revealed by multiplex Digenome-seq. Genome Res.2016;26:406-415.
- Tsai SQ, Nguyen NT, Malagon-Lopez J, Topkar VV, Aryee MJ, Joung JK.CIRCLE-seq: a highly sensitive in vitro screen for genome-wide CRISPR-Cas9 nuclease off-targets.Nat Methods.2017;14:607-614.